医薬品及びその原料について、日本・欧州・米国の各薬局方に基づき、微生物学的視点での品質検査を行っています。
主な分析内容
微生物限度試験

非無菌性の医薬品(例えば、錠剤、カプセル剤、シロップ剤、貼付剤など)及びその原料中に存在する増殖能力を有する微生物数を確認する試験を「微生物限度試験」と言います。生菌数試験は、存在する微生物を数値として計測する試験で、製品ごとに決められた数値より少なければ適合となります。特定微生物試験は、製剤の種類ごとに決められた存在してはいけない微生物を特異的に調べる試験で、該当する菌の存在が否定できれば適合となります。
- ・生菌数試験
- ・特定微生物試験
- ・培地性能試験
無菌試験
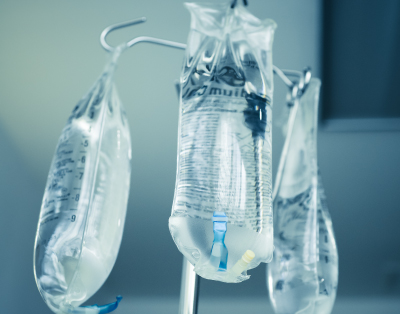
医薬品の中でも、血液や眼球に直接投与する医薬品(例えば、注射剤、輸液、点眼剤、眼軟膏剤など)は、その性質として無菌であることが求められます。これらの医薬品について、無菌であることを確認するための試験を「無菌試験」と言います。メンブランフィルター法では、微生物を捕集できるフィルターで製品をろ過し、フィルターを液体培地に漬けて培養します。直接法では、規定量の製品を液体培地に直接加えて培養します。どちらも微生物の増殖が確認されない(液体培地に濁りが認められない)場合に適合となります。
- ・メンブランフィルター法
- ・直接法
エンドトキシン試験
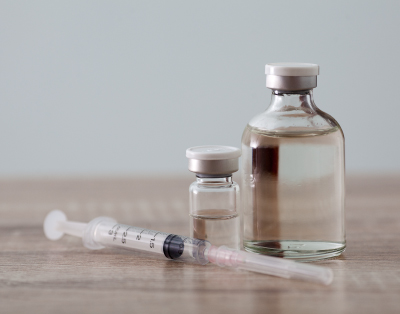
エンドトキシンとは、グラム陰性菌の細胞壁成分であり、菌が死んでいても細胞壁成分のエンドトキシンは残ってしまいます。エンドトキシンは体内に入ると発熱などの生体反応を引き起こしてしまいます。注射剤などの直接血管に投与する製剤に含まれるエンドトキシンの量が規定量以下であることを確認する試験を「エンドトキシン試験」と言います。カブトガニの血球抽出物から作られるライセート試薬とエンドトキシンが反応した際に生じる変化(ゲル化・比濁増加・黄色発色)に基づいてエンドトキシン量を計算し、規定量以下であることが確認できれば適合となります。
- ・ゲル化法
- ・比濁法
- ・比色法



